Giải bài toán một hợp chất ion cấu tạo từ ion m+ và ion x2-. Ion hoặc điện tích là nguyên tử hoặc nhóm nguyên tử mất hoặc nhận thêm electron. Một ion mang điện tích âm được gọi là anion hoặc điện tích âm khi nó nhận một hoặc nhiều điện tử, và một ion tích điện dương khi mất một hoặc nhiều điện tử được gọi là cation hoặc điện tích dương. Quá trình tạo ra các ion hoặc điện tích được gọi là quá trình ion hóa.
Một nguyên tử hoặc nhóm nguyên tử bị ion hóa được biểu thị bằng số được viết ở phía trên bên phải của ký hiệu nguyên tử hoặc nhóm nguyên tử, cho biết số lượng điện tử nhận được hoặc mất đi (nếu lớn hơn 1), và dấu + hoặc-phụ thuộc về việc nó mất hay nhận electron. Trong trường hợp chỉ mất một electron thì không cần giá trị. Ví dụ, H + hoặc Cl-.
Năng lượng ion hóa
Kim loại có xu hướng hình thành cation (mất điện tử), trong khi phi kim loại có xu hướng hình thành anion, ví dụ, natri tạo ra cation Na + và clo tạo ra anion Cl-.
Năng lượng cần thiết để tạo ra các cation bằng cách loại bỏ các điện tử từ các nguyên tử trung hòa về điện là năng lượng ion hóa. Nói chung, năng lượng ion hóa thứ n của nguyên tử là năng lượng cần thiết để loại bỏ điện tử thứ n sau khi loại bỏ điện tử thứ n trước đó.
Mỗi lần tiếp theo năng lượng ion hóa lớn hơn đáng kể so với mức trước đó. Đặc biệt, khi các êlectron ở một lớp quỹ đạo nào đó trong nguyên tử bị bứt ra thì sự thay đổi năng lượng càng tăng mạnh. Vì lý do này, các cation có xu hướng được tạo ra theo hướng loại bỏ tất cả các electron khỏi cùng một loại quỹ đạo. Ví dụ, người ta phát hiện ra rằng natri là Na +, không phải Na 2+, vì nó cần nhiều năng lượng để ion hóa. Tương tự, người ta thấy rằng magiê tồn tại ở dạng Mg2 + thay vì Mg3 +, và nhôm có thể tồn tại ở dạng cation Al3 +. Khi một nhóm nguyên tử thu nhận electron, chúng cũng trở thành ion, chẳng hạn như SO42-.
Các ion lần đầu tiên được đề xuất bởi Michael Faraday vào khoảng năm 1830 để mô tả thành phần của các phân tử chuyển động về phía anion hoặc cation. Tuy nhiên, phải đến năm 1884, Svante August Arrhenius (Svante August Arrhenius) mới mô tả cơ chế của các chuyển động này trong một luận án tiến sĩ tại Đại học Tổng hợp Uppsala University, mới được mô tả. Lý thuyết của ông lúc đầu không được chấp nhận (ông nhận bằng tiến sĩ với số điểm thấp nhất), nhưng luận án tiến sĩ của ông đã đoạt giải Nobel Hóa học năm 1903.
Một hợp chất ion cấu tạo từ ion m+ và ion x2-
Ví dụ cho khái niệm Một hợp chất ion cấu tạo từ ion m+ và ion x2- sẽ có một đề bài như dưới đây:
Một hợp chất ion gồm ion M + và ion X2- Trong phân tử M2X có 140 hạt, trong đó số hạt không mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của ion M + nhiều hơn số khối của ion X2- là 23. So với X2-, tổng số hạt trong M + là 31
- Viết cấu hình của X2- và M +
- Xác định vị trí của M và X trong bảng tuần hoàn.

Đáp án: Trong phân tử M2X có 2 nguyên tử M và 1 nguyên tử X nên tổng số hạt:
2 (2ZM + NM) + (2ZX + NX) = 140
Trong 140 hạt này, số hạt mang điện nhiều hơn số hạt không mang điện là: 44:
(2,2ZM + 2ZX) – (2NM + NX) = 44
Số khối của ion M + nhiều hơn số khối của ion X2- là 23:
(ZM + NM) – (ZX + NX) = 23
Tổng số hạt trong M + là 31 so với tổng số hạt trong X2-:
(2ZM + NM-1) – (2ZX + NX + 2) = 31
Giải phương trình trên:
ZM = 19 (K)
NM = 20
ZX = 8 (O)
NX = 8
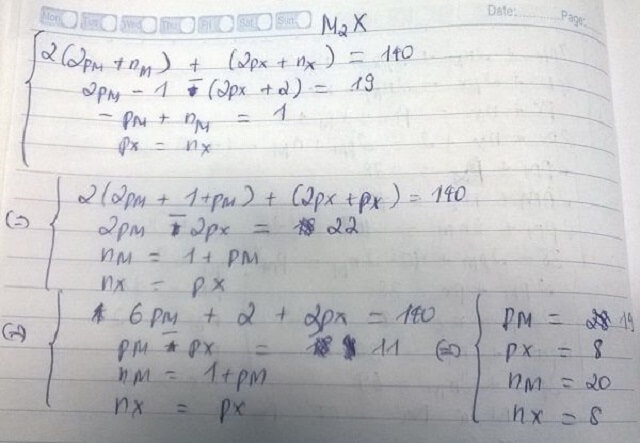
Cấu hình điện tử:
K +: 1s2 2s2 2p6 3s2 3p6
O2-: 1s2 2s2 2p6
Vị trí của K: ô 19, chu kỳ 4, nhóm IA
Vị trí của O: ô 8, chu kỳ 2, nhóm VIA
Kết
Ở bài viết trên đã có ví dụ rõ cho khái niệm Một hợp chất ion cấu tạo từ ion m+ và ion x2-. Các bạn có thể tham khảo và tìm hiểu thêm nhiều đề bài tương tự để hiểu rõ hơn
Không khí được cấu tạo bởi nhiều phân tử và nguyên tử. Khi các nguyên tử hoặc phân tử này bị mất hoặc nhận, nhiều điện tử hơn sẽ trở thành các hạt mang điện, được gọi là điện tích hoặc ion. Một ion mang điện tích dương (+) khi một ion mất một hoặc nhiều electron được gọi là cation hoặc ion dương, và ion mang điện tích âm (-) khi ion đó bẫy một hoặc nhiều electron được gọi là anion. Ion âm về bản chất là hạt mang điện âm và hạt mang điện âm (số hạt mang điện tích âm).
Ion âm hay anion là những ion âm có thể hút một hoặc nhiều điện tử khi ở trạng thái trung tính. Ion âm là những hạt có lợi, giúp tăng cường năng lượng sống nên ion âm còn được gọi là “vitamin không khí”. Nói cách khác, ion âm là nguyên tử mang điện tích âm.
